Los orbitales (S) =1=0 tiene forma esferica la extencion de este orbital depende del valor del numero cuantico principal asi un orbital 3s tiene la misma forma de orbital 2s.
Los orbitales (P) estan formados por dos lobulos identicos que se proyectan a lo largo de un eje su union de ambos concide con el nucleo atomico hay y tres orbitales p,m=-1 m=0 m=47 b a lo largo de ejes x y y.
Los orbitales (d) 1=2 tambien estan formados por lobulos hay cinco orbitales m=2-1-012.
Los orbitales (F) 1=3 tambien tienen un aspecto multio cular existen siete tipos de orbitales m=-3,-2,1,0+1+2+3
H 1s ¡
He 1s2 ¡¡!
Li 1s22s ¡¡!
B 1s22s22p ¡¡!¡¡
Be 1s2s ¡¡!¡!
C 1s22s22p2 ¡¡!¡!¡!
viernes, 7 de octubre de 2011
miércoles, 28 de septiembre de 2011
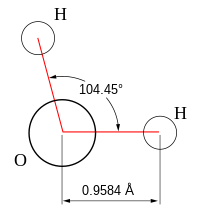
GEOMETRIA MOLECULAR
Valencia
La valencia, también conocida como número de valencia, es una medida de la cantidad de enlaces químicos formados por los átomos de un elemento químico.
Azufre - S
Fósforo - P
|
sábado, 24 de septiembre de 2011
El petróleo
El petróleo es una mezcla homogenea de compuestos orgánicos, principalmente hidrocarburos insolubles en agua. También es conocido como petróleo crudo o simplemente crudo.
Propiedades fisicas y quimicas
. Coloración: el color del petróleo varía del amarillo al rojo pardo, siendo las clases más oscuras, opacas. Los aceites de bajo peso especifico (0,777 a 0,789) son amarillos, los medianos (0,792 a 0,820) ámbar, y los aceites más pesados son oscuros. Por luz reflejada, el aceite crudo es usualmente verde, debido a la fluorescencia. Por lo general, su tonalidad se oscurece con el aumento de su peso específico, que se incrementa al aumentar su porcentaje de asfalto. Los hidrocarburos puros son incoloros, pero a menudo se colorean por oxidación, especialmente los no saturados. Los compuestos que dan color pertenecen a la clase de los hidrocarburos aromáticos; el color depende de su estructura molecular.
Olor: Es característico y depende de la naturaleza y composición del aceite crudo. Los hidrocarburos no saturados dan olor desagradable, como ocurre con los petróleos mexicanos y los de la zona vecina a Texas (Estados Unidos) debido al ácido sulfhídrico y otros compuestos de azufre. Los petróleos crudos de California, Rusia y Rumania tienen olor aromático. Los de Pensilvania tienen olor agradable a gasolina. En otros aceites el olor varía, dependiendo de la cantidad de hidrocarburos livianos y de las impurezas.
Peso específico: El petróleo es más liviano que el agua. Su peso específico es influenciado por factores físicos y por la composición química del crudo, pudiendo oscilar, en términos generales, entre 0,75 y 0,95 Kgr./lt. Aumenta con el porcentaje de asfalto.
Viscosidad: Es la medida de la tendencia a fluir, siendo de gran importancia en los aceites lubricantes y fuel-oil. Es usualmente el tiempo necesario para que un volumen dado de aceite, a una temperatura definida, fluya a través de un pequeño orificio. Se mide con viscosímetro. Todos emplean en general el mismo principio. Se controla la temperatura dentro de la taza .
Imagenes del petroleo



GEOMETRIA MOLECULAR
La geometría molecular o estructura molecular se refiere a la disposición tri-dimensional de los átomos que constituyen una molécula. Determina muchas de las propiedades de las moléculas, como son la reactividad, polaridad, fase, color, magnetismo, actividad biológica, etc. Actualmente, el principal modelo de geometría molecular es la Teoría de Repulsión de Pares de Electrones de Valencia (TRePEV), empleada internacionalmente por su gran predictibilidad.
Los alcanos son hidrocarburos, es decir que tienen sólo átomos de carbono e hidrógeno. La fórmula general para alcanos alifáticos (de cadena lineal) es CnH2n+2, y para cicloalcanos es CnH2n. También reciben el nombre de hidrocarburos saturados.
Los alcanos son compuestos formados solo por átomos de carbono e hidrógeno, no presentan funcionalización alguna, es decir, sin la presencia de grupos funcionales como el carbonilo (-CO), carboxilo (-COOH), amida (-CON=), etc. La relación C/H es de CnH2n+2 siendo n el número de átomos de carbono de la molécula, (como se verá después esto es válido para alcanos de cadena lineal y cadena ramificada pero no para alcanos cíclicos). Esto hace que su reactividad sea muy reducida en comparación con otros compuestos orgánicos, y es la causa de su nombre no sistemático: parafinas (del latín, poca afinidad). Todos los enlaces dentro de las moléculas de alcano son de tipo simple o sigma, es decir, covalentes por compartición de un par de electrones en un orbital s, por lo cual la estructura de un alcano sería de la forma:
donde cada línea representa un enlace covalente. El alcano más sencillo es el metano con un solo átomo de carbono. Otros alcanos conocidos son el etano, propano y el butano con dos, tres y cuatro átomos de carbono respectivamente. A partir de cinco carbonos, los nombres se derivan de numerales griegos: pentano, hexano, heptano...
Los alquenos u olefinas son hidrocarburos insaturados que tienen uno o varios dobles enlaces carbono-carbono en su molécula. Se puede decir que un alqueno no es más que un alcano que ha perdido dos átomos de hidrógeno produciendo como resultado un enlace doble entre dos carbonos. Los alquenos cíclicos reciben el nombre de cicloalquenos.Los alquenos, cuya fórmula general es CnH2n, pueden ser considerados como derivados de los alcanos por pérdida de dos átomos de hidrógeno en dos carbonos contiguos
Propiedades fisicas y quimicas
. Coloración: el color del petróleo varía del amarillo al rojo pardo, siendo las clases más oscuras, opacas. Los aceites de bajo peso especifico (0,777 a 0,789) son amarillos, los medianos (0,792 a 0,820) ámbar, y los aceites más pesados son oscuros. Por luz reflejada, el aceite crudo es usualmente verde, debido a la fluorescencia. Por lo general, su tonalidad se oscurece con el aumento de su peso específico, que se incrementa al aumentar su porcentaje de asfalto. Los hidrocarburos puros son incoloros, pero a menudo se colorean por oxidación, especialmente los no saturados. Los compuestos que dan color pertenecen a la clase de los hidrocarburos aromáticos; el color depende de su estructura molecular.
Olor: Es característico y depende de la naturaleza y composición del aceite crudo. Los hidrocarburos no saturados dan olor desagradable, como ocurre con los petróleos mexicanos y los de la zona vecina a Texas (Estados Unidos) debido al ácido sulfhídrico y otros compuestos de azufre. Los petróleos crudos de California, Rusia y Rumania tienen olor aromático. Los de Pensilvania tienen olor agradable a gasolina. En otros aceites el olor varía, dependiendo de la cantidad de hidrocarburos livianos y de las impurezas.
Peso específico: El petróleo es más liviano que el agua. Su peso específico es influenciado por factores físicos y por la composición química del crudo, pudiendo oscilar, en términos generales, entre 0,75 y 0,95 Kgr./lt. Aumenta con el porcentaje de asfalto.
Viscosidad: Es la medida de la tendencia a fluir, siendo de gran importancia en los aceites lubricantes y fuel-oil. Es usualmente el tiempo necesario para que un volumen dado de aceite, a una temperatura definida, fluya a través de un pequeño orificio. Se mide con viscosímetro. Todos emplean en general el mismo principio. Se controla la temperatura dentro de la taza .
Imagenes del petroleo

GEOMETRIA MOLECULAR
Geometría molecular
La geometría molecular o estructura molecular se refiere a la disposición tri-dimensional de los átomos que constituyen una molécula. Determina muchas de las propiedades de las moléculas, como son la reactividad, polaridad, fase, color, magnetismo, actividad biológica, etc. Actualmente, el principal modelo de geometría molecular es la Teoría de Repulsión de Pares de Electrones de Valencia (TRePEV), empleada internacionalmente por su gran predictibilidad.
Alcano
Los alcanos son compuestos formados solo por átomos de carbono e hidrógeno, no presentan funcionalización alguna, es decir, sin la presencia de grupos funcionales como el carbonilo (-CO), carboxilo (-COOH), amida (-CON=), etc. La relación C/H es de CnH2n+2 siendo n el número de átomos de carbono de la molécula, (como se verá después esto es válido para alcanos de cadena lineal y cadena ramificada pero no para alcanos cíclicos). Esto hace que su reactividad sea muy reducida en comparación con otros compuestos orgánicos, y es la causa de su nombre no sistemático: parafinas (del latín, poca afinidad). Todos los enlaces dentro de las moléculas de alcano son de tipo simple o sigma, es decir, covalentes por compartición de un par de electrones en un orbital s, por lo cual la estructura de un alcano sería de la forma:
donde cada línea representa un enlace covalente. El alcano más sencillo es el metano con un solo átomo de carbono. Otros alcanos conocidos son el etano, propano y el butano con dos, tres y cuatro átomos de carbono respectivamente. A partir de cinco carbonos, los nombres se derivan de numerales griegos: pentano, hexano, heptano...
Alqueno
Los alquenos u olefinas son hidrocarburos insaturados que tienen uno o varios dobles enlaces carbono-carbono en su molécula. Se puede decir que un alqueno no es más que un alcano que ha perdido dos átomos de hidrógeno produciendo como resultado un enlace doble entre dos carbonos. Los alquenos cíclicos reciben el nombre de cicloalquenos.
Alquino
Los alquinos son hidrocarburos alifáticos con al menos un triple enlace entre dos átomos de carbono. Se trata de compuestos metaestables debido a la alta energía del triple enlace carbono-carbono. Su fórmula general es CnH2n-2
lunes, 5 de septiembre de 2011
EJERCISIOS DE LAS PAGINAS 112 Y 113
1.- Dadas las siguientes disoliciones, identifica el soluto y el disolvente
1.- 5 g de NaCl + 100 g de H2O 5g de NaCl 100g de H2O
2.- 100mL de metanol +20 mL de H2O 100 mL DE metenol 20ml de H2O
3.- 500 mL de O2 +150 mL de N2 500 ml de O2 150 ml de N2
4.- 40g de Hg +20 g de Ag 20g de Ag 40 g Ag
5.- 250 mL de H2O + 10 g de azùcar 10 g de azucar 250ml de H2O
2.- Relaciona los parentesis de la derecha con los conceptos de la colomna de la izquierda
a) Disoluciòn liquida 1.- He / N2 (c )
b) Disoluciòn electrolitica 2.- azucar con agua (b)
c) Disoluciòn gaseosa 3.- amalgama ( e)
d) Disoluciòn electrolitica 4.- NaOH / agua (d)
e) Disolucion solida 5.-yodo / etanol ( a )
3.- Utiliza la siguiente informacion sobre la solubilidad de KBr y KI e indica si cada una de las disoluciones seran insaturadas saturadas o sobresaturadas.
SOLUBILIDAD g/ 100g H2O
T(ºC) KBr Kl
20 65 145
40 80 160
60 90 175
80 100 190
100 110 210
1.- 70 g KBr en 100 g H2O a 40ºC SATURADA
2.- 185g KI en 100g H2O a 60 ºC SOBRESATURADA
3.- 65g KBr en 100 g H2O a 20ºC SATURADA
4.- 180g KI en 100g H2O a 80ºC SOBRESATURADA
5.- 110g KBr en 100g H2O a 100ºC SOBRESATURADA
4.- Indica on una X si lo siguientes planteamientos aumentara o disminuira la solubilidad del NaCl (cloruro de sodio ) en agua .
Planteamiento experimental Aumenta Disminuye
NaCl ( a granel) X
Introducir el recipiente de la mezcla en agua con hielo X
Agitar la mezlca NaCl yH2O X
Calentar el vaso con NaCl y agua X
Pulverizar el NaCl antes d mezclarlo con agua X
CARACTERISTICAS DE LOS COLOIDES
Las particulas coloidales tienen propiedades intermedias entre las disoluciones verdaderas y las suspensiones .
SISTEMAS COLOIDALES
1.- Tiene masa molar alta
2.- Su tamaño no es relativamente grande
3.- Apesar de su tamaño no lo son tanto para asentarse
4.- Anivel microscopico son heterogeneas
Actualmente se sabe que los coloides son mezlcas cuyas particulas se distrubuyen de manera uniforme atravez de unmedio que actua como disolvente o medio de distribuciòn o dispersante.
Los coloids se clasifican en relaciòn con el estado de agregaciò o fisico de la fase dispersa y el medio dispersante.
Los coloides tambien pueden clasificarse en funciòn de su afinidad o repulsion con el medio de dispersion.
EJEMPLO DE COLOIDE
a) Coloides hidrafibicos ( repelen al agua) por ejemplo sustancias muy insolubles como el cloruro de plata y azufre.
b) Coloides hidrafilicos (afines alagua ) por ejemplo ala gelatina.
PROPIEDADES
Los coloides se pueden presentar otras propiedades especiales que permiten identificarlos y son:
1.- Efecto optico: La dispersion de la luz es una propiedad caracteristica de los coloides.
2.- Efecto de movimiento: Los coloides presentan un movimiento en zig_zag de forma aleatoria.
3.-Superfisie de adsorsion: Una caracteristica de los sistems coloidales es su gran superficie .
IMAGEN
1.- 5 g de NaCl + 100 g de H2O 5g de NaCl 100g de H2O
2.- 100mL de metanol +20 mL de H2O 100 mL DE metenol 20ml de H2O
3.- 500 mL de O2 +150 mL de N2 500 ml de O2 150 ml de N2
4.- 40g de Hg +20 g de Ag 20g de Ag 40 g Ag
5.- 250 mL de H2O + 10 g de azùcar 10 g de azucar 250ml de H2O
2.- Relaciona los parentesis de la derecha con los conceptos de la colomna de la izquierda
a) Disoluciòn liquida 1.- He / N2 (c )
b) Disoluciòn electrolitica 2.- azucar con agua (b)
c) Disoluciòn gaseosa 3.- amalgama ( e)
d) Disoluciòn electrolitica 4.- NaOH / agua (d)
e) Disolucion solida 5.-yodo / etanol ( a )
3.- Utiliza la siguiente informacion sobre la solubilidad de KBr y KI e indica si cada una de las disoluciones seran insaturadas saturadas o sobresaturadas.
SOLUBILIDAD g/ 100g H2O
T(ºC) KBr Kl
20 65 145
40 80 160
60 90 175
80 100 190
100 110 210
1.- 70 g KBr en 100 g H2O a 40ºC SATURADA
2.- 185g KI en 100g H2O a 60 ºC SOBRESATURADA
3.- 65g KBr en 100 g H2O a 20ºC SATURADA
4.- 180g KI en 100g H2O a 80ºC SOBRESATURADA
5.- 110g KBr en 100g H2O a 100ºC SOBRESATURADA
4.- Indica on una X si lo siguientes planteamientos aumentara o disminuira la solubilidad del NaCl (cloruro de sodio ) en agua .
Planteamiento experimental Aumenta Disminuye
NaCl ( a granel) X
Introducir el recipiente de la mezcla en agua con hielo X
Agitar la mezlca NaCl yH2O X
Calentar el vaso con NaCl y agua X
Pulverizar el NaCl antes d mezclarlo con agua X
CARACTERISTICAS DE LOS COLOIDES
Las particulas coloidales tienen propiedades intermedias entre las disoluciones verdaderas y las suspensiones .
SISTEMAS COLOIDALES
1.- Tiene masa molar alta
2.- Su tamaño no es relativamente grande
3.- Apesar de su tamaño no lo son tanto para asentarse
4.- Anivel microscopico son heterogeneas
Actualmente se sabe que los coloides son mezlcas cuyas particulas se distrubuyen de manera uniforme atravez de unmedio que actua como disolvente o medio de distribuciòn o dispersante.
Los coloids se clasifican en relaciòn con el estado de agregaciò o fisico de la fase dispersa y el medio dispersante.
Los coloides tambien pueden clasificarse en funciòn de su afinidad o repulsion con el medio de dispersion.
EJEMPLO DE COLOIDE
a) Coloides hidrafibicos ( repelen al agua) por ejemplo sustancias muy insolubles como el cloruro de plata y azufre.
b) Coloides hidrafilicos (afines alagua ) por ejemplo ala gelatina.
PROPIEDADES
Los coloides se pueden presentar otras propiedades especiales que permiten identificarlos y son:
1.- Efecto optico: La dispersion de la luz es una propiedad caracteristica de los coloides.
2.- Efecto de movimiento: Los coloides presentan un movimiento en zig_zag de forma aleatoria.
3.-Superfisie de adsorsion: Una caracteristica de los sistems coloidales es su gran superficie .
IMAGEN
viernes, 2 de septiembre de 2011
DISOLUCIONES HISOTÒNICAS
Son aquellas en donde la consentraciòn del soluto es la misma en ambos lados de la membrana de la celula por lo tanto la presiòn osmòtica en la misma disoluciòn isotonica es la misma que en los liquidos del cuerpo y no altera el vòlumen de las celulas.
Por ejemplo si se coloca un eritiocito en una disolucion isotonica retiene su volumen normal debido de que hay un flujo igual de agua, asi lo interior y exterior de la celula.
DISOLUCIÓN HIPÒTONICA
Una solución hipotónica es aquella que tiene menor concentración de soluto en el medio externo en relación al medio citoplasmático de la cèlula. Una célula sumergida en una solución con una concentración más baja de materiales disueltos, está en un ambiente hipotónico; la concentración de agua es más alta (a causa de tener tan pocos materiales disueltos) fuera de la cèlula que dentro. Bajo estas condiciones, el agua se difunde a la célula, es decir, se produce ósmosis de líquido hacia el interior de la célula.
DISOLUCIÒN HIPERTONICA
Una soluciòn hipertónica es aquella que tiene mayor concentración de soluto en el medio externo, por lo que una célula en dicha solución pierde agua (H2O) debido a la diferencia de presión, es decir, a la presiòn osmòtica, llegando incluso a morir por deshidratación. La salida del agua de la célula continúa hasta que la presión osmótica del medio externo y de la célula sean iguales.
Imajenes

DÌALISIS
Es un proceso similar a la omosis en esta una membrana, dializante permite el paso de las particulas tales tales como las moleculas e iones pequeños en soluciòn al igual que la moleculas del agua pasan atravez de ella pero retienen las particulas de mayor dimension como son los coloides.
Por lo tanto la dìalisis es un procedimiento para separar particulas en soluciones de coloide.
La dìalisis se usa para la purificaciòn de sales coloides y para algunas aplicaciones especializadas en la diferencia renal la funcion primordial del riñon eds eliminar productos de desecho mentabolico como urea y la creatina que deve eliminarse de la sangre.
Por ejemplo si se coloca un eritiocito en una disolucion isotonica retiene su volumen normal debido de que hay un flujo igual de agua, asi lo interior y exterior de la celula.
DISOLUCIÓN HIPÒTONICA
Una solución hipotónica es aquella que tiene menor concentración de soluto en el medio externo en relación al medio citoplasmático de la cèlula. Una célula sumergida en una solución con una concentración más baja de materiales disueltos, está en un ambiente hipotónico; la concentración de agua es más alta (a causa de tener tan pocos materiales disueltos) fuera de la cèlula que dentro. Bajo estas condiciones, el agua se difunde a la célula, es decir, se produce ósmosis de líquido hacia el interior de la célula.
DISOLUCIÒN HIPERTONICA
Una soluciòn hipertónica es aquella que tiene mayor concentración de soluto en el medio externo, por lo que una célula en dicha solución pierde agua (H2O) debido a la diferencia de presión, es decir, a la presiòn osmòtica, llegando incluso a morir por deshidratación. La salida del agua de la célula continúa hasta que la presión osmótica del medio externo y de la célula sean iguales.
Imajenes

DÌALISIS
Es un proceso similar a la omosis en esta una membrana, dializante permite el paso de las particulas tales tales como las moleculas e iones pequeños en soluciòn al igual que la moleculas del agua pasan atravez de ella pero retienen las particulas de mayor dimension como son los coloides.
Por lo tanto la dìalisis es un procedimiento para separar particulas en soluciones de coloide.
La dìalisis se usa para la purificaciòn de sales coloides y para algunas aplicaciones especializadas en la diferencia renal la funcion primordial del riñon eds eliminar productos de desecho mentabolico como urea y la creatina que deve eliminarse de la sangre.
Tipo de separación
Carbón vegetal y agua hterogènea
Solucíon saturada de sulfato de sodio homogènea
Yodo y arena fina heterogènea
Componentes solidos que contiene la sengre heterogènea
Colorante para alimentos y agua homegènea
Sal de mesa en disoluciòn acuos homagènea
Mezcla de hidrocarburos homogènea
Aceite comestible y agua heterogènea
Limadura de hierro y talco heterogènea
Mezcla de arena y grava heterogènea
Solucíon saturada de sulfato de sodio homogènea
Yodo y arena fina heterogènea
Componentes solidos que contiene la sengre heterogènea
Colorante para alimentos y agua homegènea
Sal de mesa en disoluciòn acuos homagènea
Mezcla de hidrocarburos homogènea
Aceite comestible y agua heterogènea
Limadura de hierro y talco heterogènea
Mezcla de arena y grava heterogènea
martes, 30 de agosto de 2011
lunes, 29 de agosto de 2011
Tlabla periodica
ELEMENTOS ORGANICOS
carbono, hidrogeno,azufre,fosforo, boro,potasio,calcio,magnesio,manganeso,hierro,cobre,zinc,cloro,sodio,cobalto,vanadio y silicio.
domingo, 28 de agosto de 2011
EJEMPLOS DE LOS CONCEPTOS: ELEMENTO, MEZCLA, COMPUESTO, DISOLUCION,COLOIDES
ELEMENTO:

El azufre, cuyo elemento químico es S, se puede encontrar como elemento libre o unido a otros elementos formando compuestos.
 La cerveza es un compuesto quimico
La cerveza es un compuesto quimico
MEZLCA HOMOGENEA:

Agua de sabor
 Pizza
Pizza

EL vinagre 
Pan de pascua La ensalada es una mezcla heterogénea, cuyos componentes pueden ser separados por medios físicos
La ensalada es una mezcla heterogénea, cuyos componentes pueden ser separados por medios físicos
Boro

Es un elemento metaloide, semiconductor, trivalente que existe abundantemente en el mineral bórax. Hay dos alótropos del boro; el boro amorfo es un polvo marrón, pero el boro metálico es negro.

El azufre, cuyo elemento químico es S, se puede encontrar como elemento libre o unido a otros elementos formando compuestos.
COMPUESTO:

MEZLCA HOMOGENEA:

Agua de sabor
 Pizza
Pizza
EL vinagre
Mezcla heterogénea

Pan de pascua
 La ensalada es una mezcla heterogénea, cuyos componentes pueden ser separados por medios físicos
La ensalada es una mezcla heterogénea, cuyos componentes pueden ser separados por medios físicosmiércoles, 24 de agosto de 2011
SISTEMAS DISPERSOS
DISOLUCIONES:
En general una disoluciom es una mezcla de por lo menos una sustancia disuelta en otra, por ejemplo, la admósfera es una disolución en general de gases entre oxígeno y nitrógeno.
las disoluciones también se clasifican de acuerdo con su condición eléctrica.
Ejemplos de disoluciones empiricas:
- Disolución insaturada: cuando a sierta temperatura,en una cantidad dadade disolvente, se tiene disuelto menos soluto del que se puede disolver en ese disolvente, se dice que la solución es insaturada
- Disolución saturada: Una solución es saturada cuando a una temperatura determinada, en una cantidad dada de disolvente, se tiene disuelta la máxima cantidad de soluto que se piede disolver.

ejercicio
a) Que tanto por ciento de agua ( H2O) de cristalización contiene,
- i) una molécula de carbonato sódico decahidratado (Na2CO3.10H2O)
ii) una molécula de ácido oxálico (etanodioico) bihidratado (C2H2O4.2H2O).
COLOIDES
Actualmente se sabe que los coloides son mezclas en las que sus partículas (fase dispersa)se distribuyen, también pueden clasificarse en función de su afinidad o repulsión con el medio de dispersión, por ello se habla de coloides liofóbicos.
Los coloides se clasifican en relación con el estado de agregación o físico de la fase dispersa y el medio dispersante.
Fase dispersa Medio dispersante Tipo Ejemplos
Liquido Líquido Emulsión Magnesia, leche, grema facial
Gas Sólido Espuma Esponja, malvavisco, unicel.
Sólido Sólido Sol sólido Aleaciones, gemas coloridas.
Propiedades de los coloides:
Los coloides pueden presentar otras propiedades especiañes que permiten idintificarlos y son:
es aleatorio y producto de las colisiones moleculares de su
partículas que describen una trayectoria en zig-zag.
SUSPENCIONES
Una suspensión es una mezcla heterogénea y es diferente a los sistemas coloidales.Una característica distintiva de las suspensiones es le tamaño de sus partículas, ya que son muy grandes y perceptibles a simple vista.
Las particulas de una suspensión son afectadas por la acción de la gravedad .
Ejemplo de suspensión

Qué volumen de solución acuosa de concentración igual a 45 mg Cu2+/cm3 sc se utilizará para preparar 250 cm3 de otra solución acuosa de concentración 2 mg Cu2+/cm3 sc?
Rta.: 11,1 cm3.
QUÍMICA 2
COMPAÑIA EDITORIAL NUEVA IMAJEN
AUTORES:Abel SalvadorLópez
Manuel Landa Barrera
lunes, 22 de agosto de 2011
ELEMENTOS COMPUSTOS MEZCLAS
¿QUE ES UN ELEMENTO?
Un elemento químico es un tipo de materia, constituida por átomos de la misma clase. En su forma más simple posee un número determinado de protones en su núcleo, haciéndolo pertenecer a una categoría única clasificada con el número atómico, aun cuando este pueda ostentar distintas masasatómicas. Es un átomo con características físicas únicas, que por tradición se define como aquellasustancia que no puede ser descompuesta mediante una reacción química, en otras más simples. No existen dos átomos de un mismo elemento con características distintas y, en el caso de que estos posean masa distinta, pertenecen al mismo elemento pero en lo que se conoce como uno de susisótopos. También es importante diferenciar entre un «elemento químico» de una sustancia simple.
¿QUE ES UN COMPUESTO?
Un elemento químico es un tipo de materia, constituida por átomos de la misma clase. En su forma más simple posee un número determinado de protones en su núcleo, haciéndolo pertenecer a una categoría única clasificada con el número atómico, aun cuando este pueda ostentar distintas masasatómicas. Es un átomo con características físicas únicas, que por tradición se define como aquellasustancia que no puede ser descompuesta mediante una reacción química, en otras más simples. No existen dos átomos de un mismo elemento con características distintas y, en el caso de que estos posean masa distinta, pertenecen al mismo elemento pero en lo que se conoce como uno de susisótopos. También es importante diferenciar entre un «elemento químico» de una sustancia simple.
¿QUE ES UN COMPUESTO?
un compuesto es una sustancia formada por la unión de dos o más elementos de la tabla periódica. Una característica esencial es que tiene una fórmula química. Por ejemplo, el agua es un compuesto formado por hidrógeno yoxígeno en la razón de 2 a 1 (en número de átomos).
En general, esta razón fija es debida a una propiedad intrínseca. Un compuesto está formado por moléculas o iones conenlaces estables y no obedece a una selección humana arbitraria. Por este motivo el bronce o el chocolate son denominadas mezclas o aleaciones, pero no compuestos.
Los elementos de un compuesto no se pueden dividir o separar por procesos físicos (decantación, filtración, destilación, etcétera), sino sólo mediante procesos químicos.
¿QUE ES UNA MEZCLA?
una mezcla es un sistema material formado por dos o más sustancias puras pero no combinadas químicamente. En una mezcla no ocurre una reacción química y cada uno de sus componentes mantiene su identidad y propiedades químicas. No obstante, algunas mezclas pueden ser reactivas, es decir, que sus componentes pueden reaccionar entre sí en determinadas condiciones ambientales, como una mezcla aire-combustible en un motor de combustión interna.
Los componentes de una mezcla pueden separarse por medios físicos como destilación, disolución, separación magnética, flotación, filtración, decantación ocentrifugación. Si después de mezclar algunas sustancias, éstas reaccionan químicamente, entonces no se pueden recuperar por medios físicos, pues se han formado compuestos nuevos. Aunque no hay cambios químicos, en una mezcla algunas propiedades físicas, como el punto de fusión, pueden diferir respecto a la de sus componentes.
Las mezclas se clasifican en homogéneas y heterogéneas. Los componentes de una mezcla pueden ser sólidos, líquidos o gaseosos.
Suscribirse a:
Entradas (Atom)